§ 1.4.1. Распределение молекул газа по скоростям
При соударениях друг с другом или со стенками вакуумной камеры молекулы газа изменяют свои скорости как по величине, так и по направлению. Пользуясь гипотезами о существовании стационарного распределения молекул по скоростям и об изотропности пространства газовых молекул, а также учитывая, что. согласно (1.11), среднеквадратичная скорость V KB = V3kT/m, Максвелл получил функцию распределения молекул по скоростям:
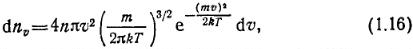
где dn v число молекул, скорости которых заключены в пределах от v до v+dv.
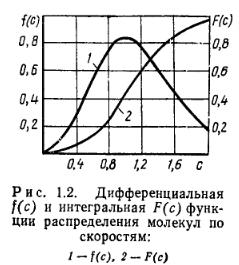
Скорость, при которой наблюдается максимум функции распределения, называется наиболее вероятной скоростью:
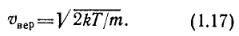
Если ввести обозначение С=v/vвep, то формулу (1.16) можно переписать так:
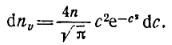
Безразмерные функции f (с) = dnv/ (dne) и F (с)= f (с) de представлены на рис, 1.2. Функция Р(е) численно равна доле общего числа молекул, скорости которых не превышают с.
В вакуумных расчетах часто используют скорости:
Среднеарифметическую:
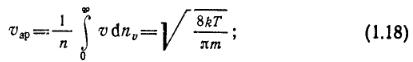
среднеквадратичную
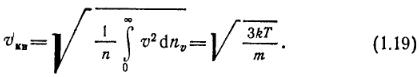
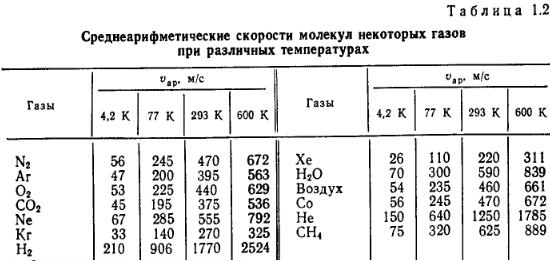
Соотношение между скоростями vвер, vар и vкв равно 1: 1,128:1,225, Так, указанные скорости для молекул азота при ООС составляют и ве р=402 м/с, и ар=453 м/с, и кв =492 м/с. Среднеарифметические скорости молекул некоторых газов при различных температурах приведены в табло 1.2.
Согласно (1.14), для воздуха при Т=З00 К и М=29 кг/кмоль при атмосферном давлении поток газовых молекул N =29*10 23 см-2c-1, а из (1.15) объем молекул, ударяющихся единицу поверхности в единицу времени, Vq=11,6.103 м3 /(с см \2).
Преобразуя (1.16), получим функцию распределения молекул по энергиям:
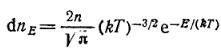
Здесь E= mvкв 2/2 энергия f(x) поступательного движения молекулы; dnE число молекул, энергия которых лежит в интервале от Е до Е +dE. Вводя переменную х=Е/ (kT), получим
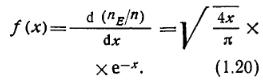
Интегральная кривая, представляющая собой долю молекул газа, энергия которых меньше Е, определяется функцией
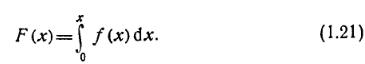
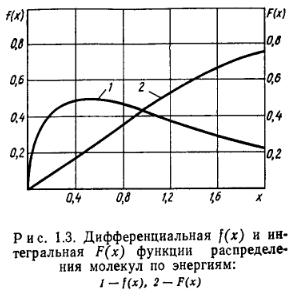
На рис, 1,3 в безразмерной форме представлены графики функций (1,20) и (1,21), Максимум дифференциальной кривой соответствует наиболее вероятной энергии Евер=0,5 kT. Расчет среднеарифметического значения энергии молекул дает Еар= 1,5 kT,
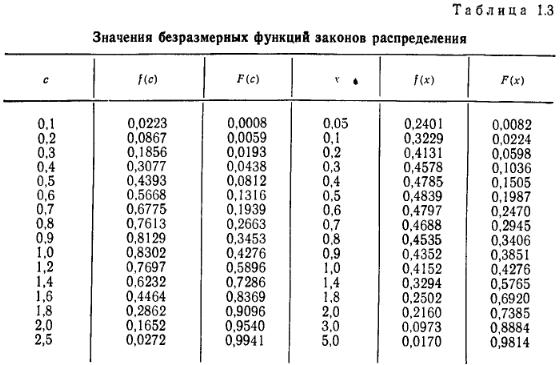
Наиболее важные значения безразмерных функций даны в табл. 1.3.