Глава 1. Кристаллические дисперсные материалы как объект сушки
Кристаллические дисперсные материалы могут быть органического и неорганического происхождения. К ним относится большой класс минеральных солей (соли натрия, калия, бария, йода, марганца, сульфаты, сульфиды), органические соединения (сахар-песок, пищевые кислоты — лимонная, винная, щавелевая,—нафталин, веронал и др.), минеральные удобрения, фармацевтические препараты. Большинство из них хорошо растворяется в воде и увеличивает степень растворимости с повышением температуры. Часть материалов чувствительна к недопустимому превышению температуры, меняя при этом внешний вид, физико-химические свойства, структуру. Так как сушка влажных материалов, в том числе и кристаллических дисперсных, является не только теплофизическим, но и технологическим процессом, то последний должен быть таким образом организован, чтобы сохранить, а в некоторых случаях даже улучшить свойства материала. Так, например, при сушке хлористого калия (флотоконцентрат) необходимо сохранить амины жирного ряда, присутствие которых в значительной степени препятствует слеживаемости хлористого калия при его хранении. Последнее обстоятельство повышает эффективность использования удобрений при их внесении в почву. Недопустимые превышения температуры материала и времени его выдержки в зоне сушки могут привести к порче продукта (карамелизация сахара) или ухудшению его товарных свойств (растрескивание кристаллов).
В большинстве случаев конечная влажность кристаллических материалов невелика и составляет доли процента. Это обусловливается способностью минеральных солей при повышенной влажности слеживаться, а в органических соединениях, кроме этого, могут происходить процессы разложения и порчи продуктов при их хранении.
Характерной особенностью рассматриваемых материалов является также то, что размер частиц колеблется от нескольких микрон до нескольких миллиметров и, следовательно, при их сушке неизбежно возникает проблема уноса мелких частиц. Иногда унос материала практически недопустим из-за его токсичности (например, для перманганата калия).
Рассматриваемые материалы могут иметь различную кристаллическую структуру—кубическую, в виде октаэдров, призм и т. д. Их можно разделить на две группы: материалы, не имеющие в своем составе химически связанной воды, и имеющие эту связь—кристаллогидраты. Вода, входящая в кристаллогидраты, является самостоятельной единицей их кристаллической решетки. Прочность связи между веществом и кристаллизационной водой в кристаллогидратах весьма различна. Одни из них теряют кристаллизационную воду уже при комнатной температуре (Na2CO3- 10H2O), обезвоживание других требует довольно высокой температуры (прокаливание). Иногда удаление кристаллизационной воды нежелательно (например, для лимонной кислоты), так как при этом теряются некоторые свойства материала.
Свойства кристаллогидратов несколько отличаются от аналогичных свойств безводных кристаллических дисперсных материалов (они имеют повышенную слеживаемость, комкуемость). Естественно, что энергия связи влаги с материалом для кристаллогидратов и безводных кристаллов существенно различна. Следовательно, для рационального выбора того или иного способа сушки влажного материала необходимо знать его гигроскопические свойства.
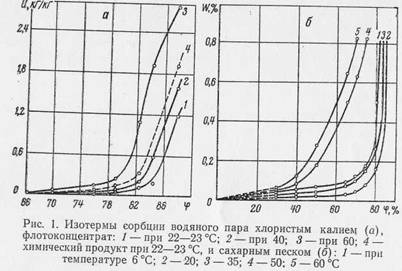
Гигроскопичность различного рода удобрений была исследована П. А. Барановым [1] и Н. Е. Пестовым [37]. Однако они не получили изотерм сорбции и не рассматривали вопросы, связанные с изучением связи влаги с материалом. Изотермы сорбции кристаллических водорастворимых дисперсных материалов впервые были получены в работах [60, 61]. Исследовались гигроскопические свойства хлористого калия (КС1) тен-зиметрическим методом при температурах воздуха 22—23, 40 и 60 °С.
Как видно из рис. 1, а, для хлористого калия заметное поглощение влаги имеет место лишь при ф>66%, причем с увеличением влажности воздуха до определенного значения сравнительно не намного увеличивается влагосодержание материала, а начиная с £/=0,2 кг/кг независимо от температуры направление кривойU=f(q>) резко меняется, что связано с изменением механизма поглощения влаги.
Механизм поглощения влаги можно представить следующим образом [37, 61]. Вначале идет процесс моно- и полимолекулярной адсорбции, затем заполнение влагой капилляров, образованных трещинами и щелями в кристаллах, и растворение соли в поглощенной воде; раствор постепенно начинает распространяться по поверхности тела, и дальнейшее поглощение влаги осуществляется насыщенным раствором соли, т. е. происходит процесс абсорбции. В этот же момент направление кривой изотермы сорбции изменяется. В работе [61] дана также зависимость, аппроксимирующая участок изотермы сорбции от ф = 66% до ф = 85%, имеющий наибольшую практическую ценность.
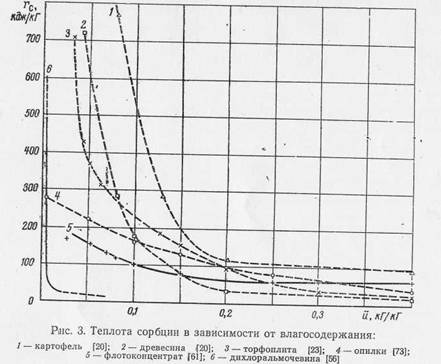
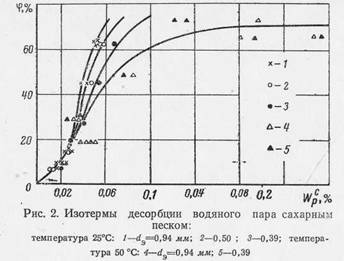
Эксперименты показали, что максимальная гигроскопическая влажность для водорастворимых веществ уже не является границей, характеризующей гигроскопическое и влажное состояние материала, как это имеет место для других капил-лярнопористых тел. По изложенной в работе [60] методике были выполнены также исследования гигроскопических свойств сахара-песка [31, 52]. В работе [31] были построены изотермы сорбции водяного пара сахарным песком для температур 6, 20, 35, 50, 60 °С (рис. 1, б), при этом установлено, что при прочих равных условиях равновесная влажность сначала уменьшается (от 6 до 20 °С), а потом увеличивается (от 20 до 60 °С). Изотермы десорбции для сахара-песка были получены И. Б. Ткаченко (Новицкой) [55] тензиметрическим методом. Опыты были проведены для температур 20 и 50 °С для нескольких фракционных составов сахарного песка (эквивалентные диаметры при этом равнялись 0,94, 0,5, 0,39 мм)(рис. 2). Анализ изотерм десорбции показал, что температура оказывает заметное влияние на величину равновесной влажности, особенно при больших значениях ф. Исследования по гигроскопическим свойствам тростникового сахара-сырца изложены в работе [50]. Изотермы сорбции и десорбции позволяют не только качественно оценить формы связи влаги с материалом, но и определить величину энергии этой связи, обусловливающей в большой степени выбор метода сушки. Из анализа изотерм сорбции и величин энергии связи влаги с материалом (рис. 3) видно,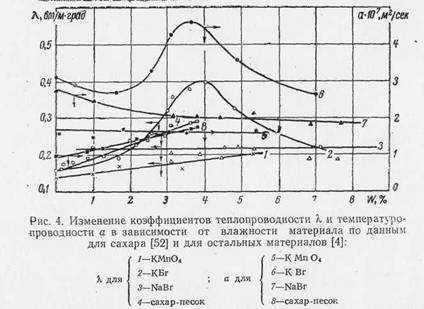 что кристаллические дисперсные материалы имеют слабую связь влаги с материалом, поэтому для их сушки нужно применять такие методы, которые характеризуются высокой интенсивностью сушки при сравнительно незначительном времени пребывания материала в зоне сушки. При расчете процесса сушки влажных, в том числе и кристаллических дисперсных материалов, необходимо знать их теплофизические свойства, особенно зависимости этих свойств от температуры и влажности материала.
что кристаллические дисперсные материалы имеют слабую связь влаги с материалом, поэтому для их сушки нужно применять такие методы, которые характеризуются высокой интенсивностью сушки при сравнительно незначительном времени пребывания материала в зоне сушки. При расчете процесса сушки влажных, в том числе и кристаллических дисперсных материалов, необходимо знать их теплофизические свойства, особенно зависимости этих свойств от температуры и влажности материала.
При расчете процесса сушки влажных, в том числе и кристаллических дисперсных материалов, необходимо знать их теплофизические свойства, особенно зависимости этих свойств от температуры и влажности материала. Источника тепла постоянной мощности. Как видно из рис. 4, для перманганата калия и сахарного песка (кривые 1, 4) коэффициент теплопроводности линейно возрастает с увеличением влажности, так же как и для других дисперсных материалов 158]. Для бромистого натрия (кривая 3) коэффициент теплопроводности в исследуемом диапазоне влажности W=0-9% не зависит от последней. Авторы [4] объясняют это особенностью поглощения влаги бромистым натрием, частицы которого представляют собой смесь агломератов из мельчайших кристаллов. Поэтому при увлажнении NaBr влага поглощается в первую очередь мельчайшими капиллярами, которые пронизывают описанные выше агломераты, а вследствие образования би-гидрата NaBr *2H2O до определенной влажности на поверхности частиц не появляется пленка насыщенного раствора, способствующая улучшению контакта между частицами, как это имеет (NaBr, KBr, КМпО4) по методу плоского для большинства водорастворимых кристаллических дисперсных материалов. Характер изменения коэффициента теплопроводности бромистого калия в зависимости от влажности резко отличается от изменения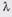 для других материалов при неизменной температуре. Кривая 2 (рис. 4) имеет максимум при
для других материалов при неизменной температуре. Кривая 2 (рис. 4) имеет максимум при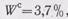 что неоднократно было подтверждено экспериментальными исследованиями [4]. Основное влияние на характер изменения коэффициента температуропроводности перечисленных выше материалов от влажности (рис. 4, кривые 5, 6, 7, 8) оказывает коэффициент теплопроводности. Теплоемкость исследованных материалов, как показали эксперименты, имеет линейную зависимость от влажности и хорошо описывается известной формулой [58].
что неоднократно было подтверждено экспериментальными исследованиями [4]. Основное влияние на характер изменения коэффициента температуропроводности перечисленных выше материалов от влажности (рис. 4, кривые 5, 6, 7, 8) оказывает коэффициент теплопроводности. Теплоемкость исследованных материалов, как показали эксперименты, имеет линейную зависимость от влажности и хорошо описывается известной формулой [58].
